Existe una conexión entre los gliomas, un tipo de tumor cerebral que es resistente a quimioterapia y radioterapia, y las enfermedades neurodegenerativas, tal y como revela un estudio realizado por la Unidad Funcional de Investigación de Enfermedades Crónicas del Instituto de Salud Carlos III (ISCIII), en colaboración con investigadores del CIBERNED, del CIBERONC, de la Asociación Española de contra el Cáncer (AECC), del Centro de Biología Molecular del CSIC y del Hospital 12 de Octubre, integrados en el Instituto de Investigación Sanitaria i+12.
Entre sus conclusiones, los investigadores destacan que este hallazgo supone un punto de partida muy importante para el diseño de nuevas estrategias terapéuticas para el tratamiento en este tipo de cáncer. El trabajo, que ha sido publicado en Science Translational Medicine, demuestra que la proteína TAU, que tradicionalmente se ha relacionado con diversas patologías degenerativas en el cerebro, está presente en las células de los gliomas. En estos tumores, la proteína TAU estaría regulando la capacidad que tienen las células tumorales para promover la formación de nuevos vasos sanguíneos, que son fundamentales para el crecimiento de este tipo de cáncer.
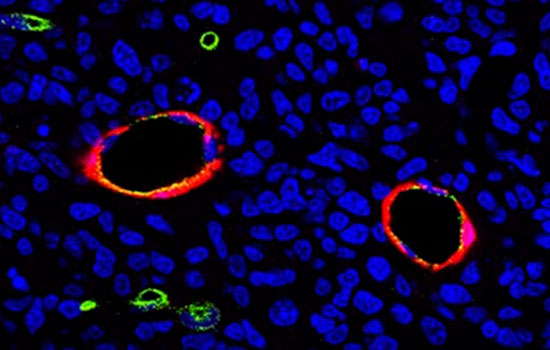
Tal y como destacn desde la Unidad Funcional de Investigación de Enfermedades Crónicas del Instituto de Salud Carlos III, la investigación permite conocer mejor los gliomas, un tipo de cáncer poco frecuente pero con una de las tasas de mortalidad más elevadas, que representa alrededor del 60% de las neoplasias cerebrales. Estos tumores deben su nombre a su similitud con las células de glía, que están presentes en el sistema nervioso central y que dan soporte a las neuronas. Además, los pacientes que son diagnosticados con los gliomas más agresivos tienen un índice de supervivencia muy bajo, de en torno a 15 meses.
Además, el estudio abre una nueva vía para la búsqueda de tratamientos que pudieran ser utilizados para controlar este tipo de tumores, los más agresivos dentro de los tumores cerebrales. El trabajo se basa en la caracterización de muestras tumorales de pacientes con gliomas, así como en el estudio de diversos modelos preclínicos, tanto con cultivo de células tumorales como con modelos animales.
Los resultados muestran que la proteína TAU está presente en los gliomas menos agresivos y que su expresión se pierde a medida que aumenta el grado de malignidad del tumor. Por ello, los datos sugieren que TAU podría servir también como un marcador de buen pronóstico para los pacientes. Los investigadores también han demostrado que TAU reprime la capacidad que tienen las células de glioma de promover la formación de nuevos vasos sanguíneos. Estos vasos sanguíneos tumorales son diferentes de los vasos normales en el cerebro y son fundamentales para proveer de nutrientes a las células del glioma, favoreciendo un crecimiento más agresivo. De hecho, los resultados demuestran que existe una correlación inversa entre la presencia de TAU en los tumores y la cantidad de vasos sanguíneos ‘aberrantes’ en los mismos.
Otra conclusión relevante del estudio es que la función de la proteína TAU en los gliomas se puede imitar con compuestos derivados del taxol, que ya se utilizan como agentes antitumorales en otros tumores y que producen un efecto aditivo con la quimioterapia convencional de los gliomas. Este hallazgo podría abrir la puerta a nuevas terapias basadas en el empleo de estos compuestos, o incluso en el uso de fármacos que hubieran sido inicialmente diseñados para pacientes con enfermedades neurodegenerativas.
En este sentido, este trabajo de investigación, que ha contado con financiación del Ministerio de Economía y Competitividad, de la Asociación Española contra el Cáncer y del NIH (National Institutes of Health), también podría tener importantes implicaciones para caracterizar nuevas funciones de la proteína TAU en dichas patologías degenerativas, donde ya existen evidencias de la relevancia que podría tener la vasculatura cerebral de los pacientes en la evolución de la enfermedad.
Referencia del estudio:
R. Gargini, B. Segura-Collar, B. Herránz, V. García-Escudero, A. Romero-Bravo, F. J. Núñez, D. García-Pérez, J. Gutiérrez-Guamán, A. Ayuso-Sacido, J. Seoane, A. Pérez-Núñez, J. M. Sepúlveda-Sánchez, A. Hernández-Laín, M. G. Castro, R. García-Escudero, J. Ávila, P. Sánchez-Gómez, The IDH-TAUEGFR triad defines the neovascular landscape of diffusen gliomas. Sci. Transl. Med. 12, eaax1501 (2020)


